Säkerhet och tolerabilitet för RAVICTI® (glycerolfenylbutyrat) 1,2
RAVICTI® är väldokumenterat vid behandling av ureacykelrubbningar
De vanligaste rapporterade biverkningarna (>5 %) under RAVICTI-behandling var:
- Diarré (8,8 %)
- Flatulens (8,8 %)
- Huvudvärk (8,8 %)
- Nedsatt aptit (7,0 %)
- Kräkningar (6,1 %)
- Trötthet (5,3 %)
- Illamående (5,3 %)
- Onormal hudlukt (5,3 %)
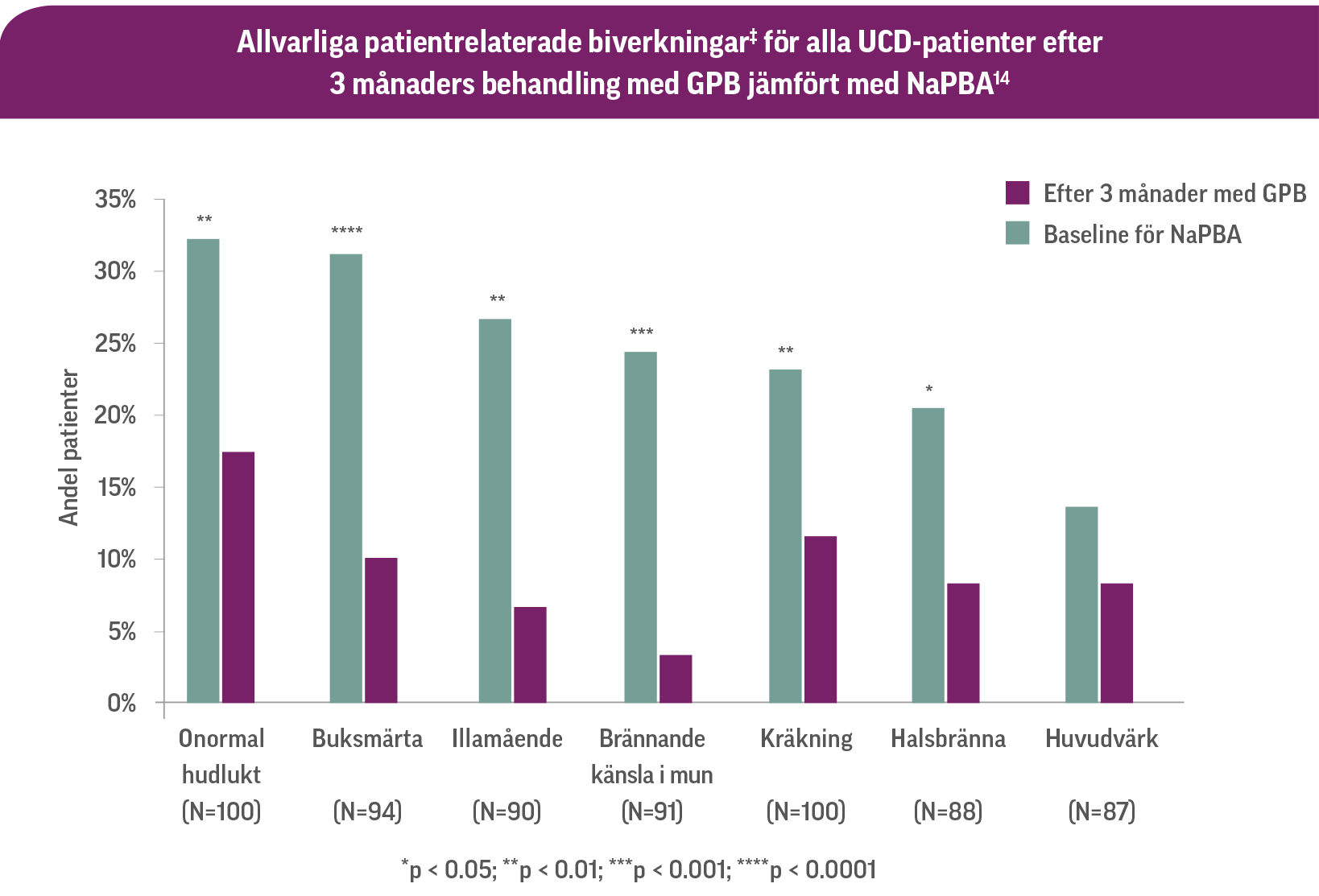
Behandlingsrelaterade biverkningar – RAVICTI vs NaPBA
Hundra patienter eller deras vårdgivare fick svara på ett icke validerat UCD-specifikt frågeformulär som innehöll en fördefinierad lista över vanliga symtom i samband med ”nitrogen scavengers”. Baseline-värden (medan patienterna fick natriumfenylbutyrat [NaPBA]) jämfördes med värden efter tre månaders behandling med glycerolfenylbutyrat (GPB).3
Varningar och försiktighet
- Överkänslighet mot den aktiva substansen.
- Behandling av akut hyperammonemi.
Den dagliga dosen ska justeras individuellt efter patientens skattade ureasynteskapacitet, om sådan finns, aminosyraprofil, proteintolerans och behov av dagligt proteinintag i kosten för att främja tillväxt och utveckling. Tillskott av aminosyraberedningar kan vara nödvändiga för att hålla de essentiella aminosyrorna och de grenade aminosyrorna inom det normala intervallet. Ytterligare justeringar kan baseras på övervakning av plasmanivåer av ammoniak, glutamin, U-PAGN och/eller plasmanivåer av PAA och PAGN samt PAA-till-PAGN-förhållandet i plasma (se avsnitt 4.2).
Kortikosteroider
Användning av kortikosteroider kan orsaka nedbrytning av kroppsprotein och öka plasmanivåerna av ammoniak. Övervaka ammoniaknivåerna noggrant när kortikosteroider och glycerolfenylbutyrat används samtidigt.
Valproinsyra och haloperidol
Hyperammonemi kan induceras av haloperidol och av valproinsyra. Övervaka noggrant ammoniaknivåerna när användning av valproinsyra eller haloperidol är nödvändigt hos UCD-patienter.
Probenecid
Probenecid kan hämma den renala utsöndringen av metaboliter av glycerolfenylbutyrat, inklusive PAGN.
Fertila kvinnor ska använda effektiv preventivmetod (se avsnitt 4.6).
Säkerhetsrapportering och produktklagomål
Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning. Rapporteringsformulär och information finns på: www.läkemedelsverket.se. Biverkningar bör också rapporteras till Immedica via e-post: safety@immedica.com
Om du vill rapportera ett produktklagomål ska detta rapporteras enligt nationella krav och i första hand till ditt lokala apotek. Du kan också kontakta Immedica Quality på: complaints@immedica.com
Referenser:
1. RAVICTI European Assessment Report.
2. Summary of Product Characteristics RAVICTI.
3. Nagamani SC et al. Mol Genet Metab. 2015;116:29–34.